
自然科学総合実験 (化学分野を担当します)
最新の更新日: 2012/Oct/21
無機定性分析 Fe、Al、 Zn、Co
万一、薬品が眼に入ったら非常に危険 (失明の恐れもあり)なので、保護メガネは必ず着用し、 ドラフトの遮蔽ガラスを下ろす。
Fe3以外の一般重金属を含む廃液は、黄色テープを巻いた三角フラスコに
実験-10、検出反応-4 で、Fe3+イオンを 検出するとすぐに色が消えてしまう。
実験ノート・筆記具と Fe3+イオンが入った試験管を持って 教卓にて検出し、ただちに結果を教官に見せ、廃液を瓶Ⅰに捨て、ノートに記入する。 他イオンの検出チェックより Fe3+イオンの確認を優先します
SCN- が入った溶液は毒性が高いため、すぐに 瓶Ⅰに捨てる。試験管に1cm3程度のイオン交換水をスポイトで試験管に接しないように入れ、
すすぎ水も瓶Ⅰに捨てる。さらに試験管に1cm3程度のイオン交換水をいれ、このすすぎ水も瓶Ⅰに捨てる。

それぞれの検液の色を観察し、ノートに記録(次回、第4回実習で 未知検液を扱う際のヒント)
 実験-8: 実験-7でできた沈殿をHNO3で溶かす際、ろ過綿が黒いのは沈殿が溶けていない状態。
実験-8: 実験-7でできた沈殿をHNO3で溶かす際、ろ過綿が黒いのは沈殿が溶けていない状態。
沈殿の部分が熱水浴に浸かるよう、ビーカーの液量を管理し、十分に時間をかける。
黄褐色のゲル状沈殿が、濃NH3水を十分に加えてもできないなら、さらに濃NH3水を加えて加熱。
その前の操作で 残っているろ過綿、試験管のろ液、蒸発皿の回収残り に まだ残っている可能性が高いので、
使った器具・実験ノートをスタッフに示して、相談してください。 リカバリ-できる ことが多いです。
◆ 確認反応を うまくやる コツ
実験-10 Feの検出: 時間が経つと色が消えてしまうので、すぐに教官に見せる
実験-11 Alの検出: テキストの指示でうまくいかないとき、さらに CH3COOHを2滴加え、10~15分加熱
実験-13 Coの検出: テキストの指示でうまくいかないとき、(NH4)2CO3 を数滴加え、さらに加熱
実験-14 Zn の検出: ジンコン の結晶は、多すぎてはダメ。 (これらのヒントは次回にも役立ちます)
結果を報告する際 Feを除く、3本の試験管が それぞれ どのイオンなのかを、実験ノートと共に示すこと!
レポートは、実験結果のレポートと、巻末問題の解答を別々に綴じ、それぞれに学籍番号と氏名を記入する。
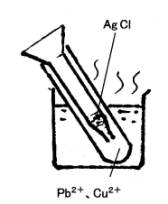
無機定性分析 Ag, Pb、Cu の分離検出で、 テキストにはない 追加資料 (火曜AM 向 )
*要確認 ドラフトの操作—スイッチ・照明・遮蔽ガラス
試験管の洗浄方法(教官卓上で説明)
薬液の場所 -- 試料・共通検出試薬・補充用・ホルマリン・イオン交換水
廃液タンク
緊急シャワー
ろ過管と加圧バルブの操作 -- 教官卓上で説明を受けてから、各自で 実験前に練習
① ろ過綿を指で丸めて、ミクロカキマゼ棒の細いほうでろ過管に詰め、ミクロカキマゼ棒の太いほうで押さえ、
(ろ過綿が緩すぎると、沈殿がろ液と一緒に試験管に落ちてしまう)
② 空の試験管で、ろ過管を受ける。
③ ろ過管に、スポイトで水を入れる。
④ 緩めた加圧バルブをろ過管に押し当てから、加圧バルブを抑えて(圧力を加えて) 水を押し出す
×(加圧バルブで、ろ過綿を吸い上げたら失敗)
スポイド ― 垂直にしてゴムを親指と人差指の間で押す。 滴下は試験管の真上から、試験管に接触させない

実験の前に
0) 保護メガネは、引き出しから取り出して必ず着用。 万一、薬品が眼に入ったら非常に危険(失明の恐れあり)
1) ビーカーに、水浴用の温水を用意。 スポイトを入れた太ガラス管にはイオン交換水を入れておく
2) 試験管をイオン交換水で洗浄
3) スポイトに 1cm3 の標線があるので、“何滴が1cm3 になるか”、を確認してテキストの滴数を換算。
4) 薬品は常に目より低い位置で扱う。 滴瓶の首を持って机上に移動し、首を押さえてスポイトをもう一方の手で操作する。
使用後は元の位置に戻す。 量が少なくなったら補充。
同じ薬品でも濃度が違うものがあるので要注意 (瓶に巻いたテープの色で区別しています)。
5) 重金属を含む廃液は、黄色いテープを巻いた三角フラスコに溜めておいて、最後に教卓右側の黄色いテープを巻いたポリタンクに捨てる。
三角フラスコは午後のグループが使うので洗浄不要。
6) 質問の際は、どの実験でどんな操作したのか、“実験ノートを示して、わからないことを整理” してから

実験のポイント
 それぞれの金属イオン検液の色を観察し、ノートに記録(第4回実習で 未知検液を扱う際のヒント)
それぞれの金属イオン検液の色を観察し、ノートに記録(第4回実習で 未知検液を扱う際のヒント)
実験-1: まず、洗浄用の1cm3 の熱水を準備しながら、実験を進める
(洗浄用の熱水が冷めていたら、Pb Cl2 が解けにくい。
そこで、ろ過管ごと熱水浴に漬けてから
両手に軍手をはめて、熱いうちに加圧バルブで Pb 2+ が含まれるろ液を押し出す。
ろ液が冷えると Pb Cl2 が析出することがある)
実験-3 : Pb Cl2 の沈殿が確認できないなら、実験-1で操作ミスかも。 蒸発凝縮は水浴上で
H2S は有毒なので、綿で緩く栓をして イオン交換水で湿らせて捕集する
実験-4 : [Cu(NH3)4]2+ の色は? (Cu が、ろ液中に存在することを確認)
教官に結果を報告する際、
1) 3本の試験管を見せる際、それぞれ どのイオンなのか、
2) 実験-2で a), b), c) のAgの検出法で どれを使ったのか、を実験ノートと共に示し、確認スタンプをもらう!
レポートは、実験結果のレポートと、巻末問題の回答を別々に綴じる
科学実験講義
テキスト、page9、 図7がわかりにくいので、下図を参照
担当する芸工生向けには、他の班・曜日とは 別バージョンの説明パワポを使用します

*関連ページに移動するには、⇒ にマウスを移動し、クリックしてください
Counter :