塩酸(えんさん)の電気分解について
【電気分解とは】 水溶液に電流を流すと、水溶液に溶けている物質が化学変化を起こして別の物質 になることがある。 水溶液に電流を流して物質を分解することを電気分解(でんきぶんかい)という。 |
【塩酸(えんさん)とは】 塩化水素(えんかすいそ)という気体を水に溶かした水溶液が塩酸(えんさん)である。 塩酸(えんさん HCl)は、水溶液中でH+(水素イオン)とCl−(塩化物イオン)に 分かれている。これを塩酸(えんさん)の電離(でんり)という。式で表すと、 HCl → H+ + Cl− 塩 酸 水素イオン 塩化物イオン となる。 |
【塩酸(えんさん)の電気分解の様子】 塩酸(えんさん)に電流を流すと、 +極(陽極 ようきょく)から塩素(Cl2 えんそ) −極(陰極 いんきょく)から水素(H2 すいそ) という気体が発生する。 |
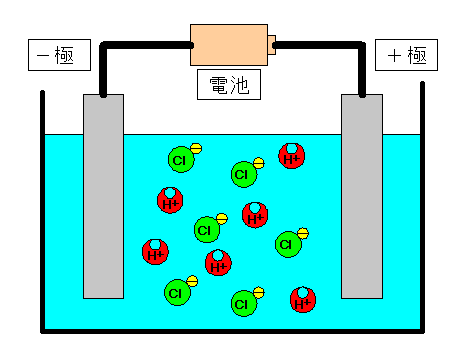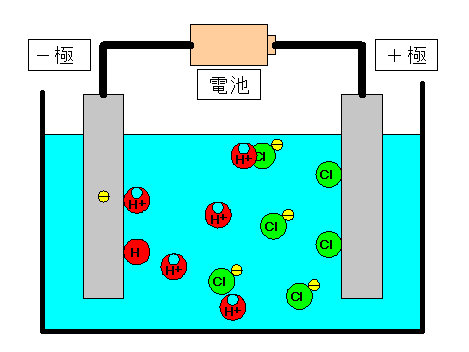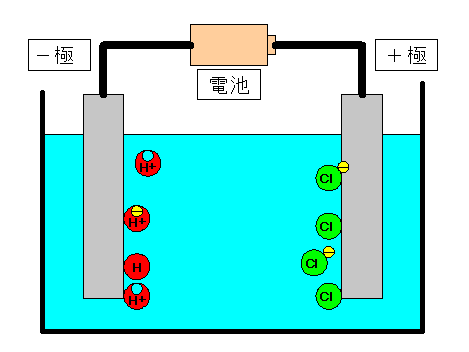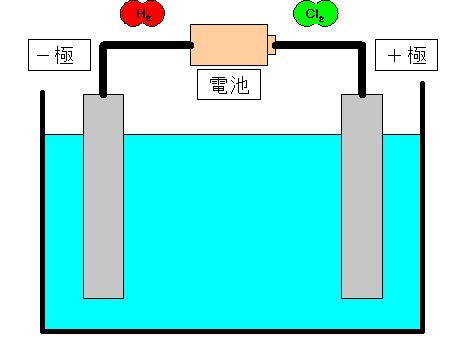
〈 塩酸(えんさん)の電気分解の様子 〉
| 水溶液の中でのイオンの動きの様子 | 説 明 |
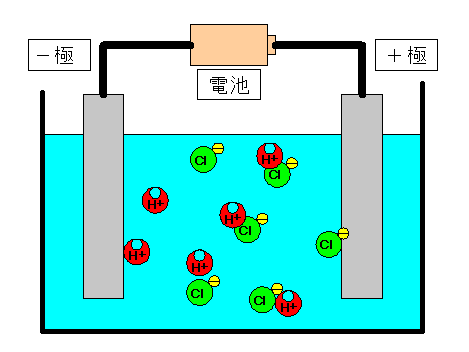 |
塩酸に電圧を加えると、 水素イオン(H+)は−極(陰極)へ移動する。 塩化物イオン(Cl−)は+極(陽極)へ移動する。 |
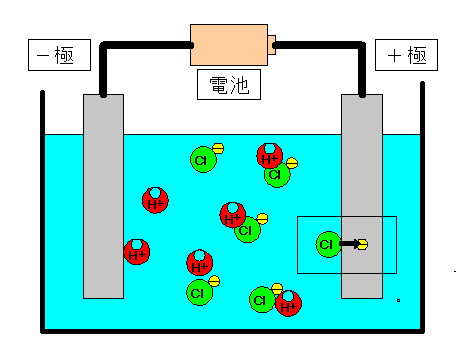 |
塩化物イオン(Cl−)が余分にもっていた電子1個を+極(陽極)にわたし、塩素原子にもどる。 |
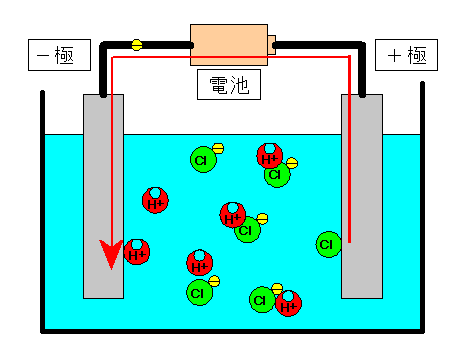 |
電子が+極(陽極)から−極(陰極)へ移動する。 |
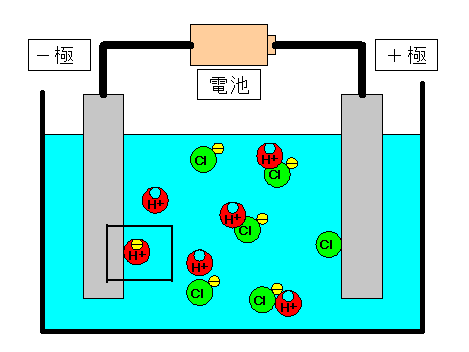 |
水素イオン(H+)が−極(陰極)でその電子を受け取り、水素原子にもどる。 |
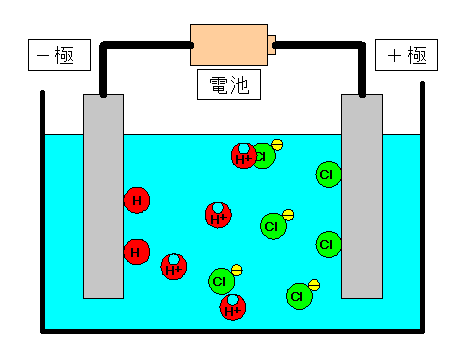 |
同じくり返しが続く。 +極(陽極)に塩素原子が2個できる。 −極(陰極)に水素原子が2個できる。 |
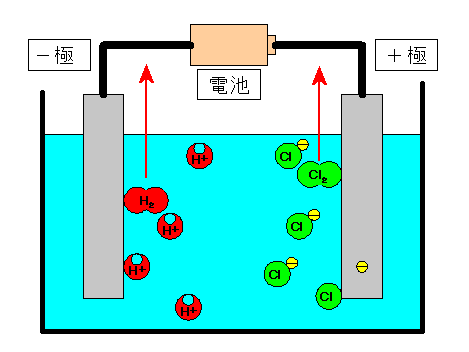 |
+極(陽極)では塩素原子どうしがくっつき塩素分子(Cl2)ができる。 −極(陰極)では水素原子どうしがくっつき水素分子(H2)ができる。 |
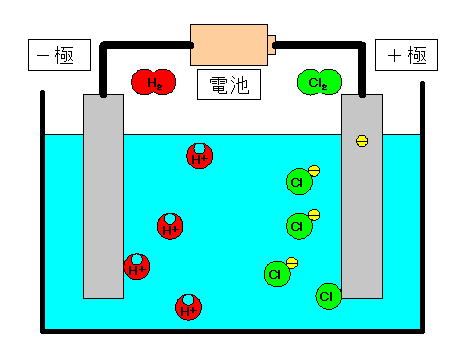 |
+極(陽極)では塩素分子(Cl2)が気体となって発生する。 −極(陰極)では水素分子(H2)が気体となって発生する。 |
【電極(でんきょく)でのイオンの変化の様子】 +極(陽極) 2Cl− → Cl2↑ + 2 塩化物イオン2個 塩素発生 電子2個  電子の移動 −極(陰極) 2H+ + 2 水素イオン2個 電子2個 水素発生 ※ ↑は気体が発生することを意味する。 |